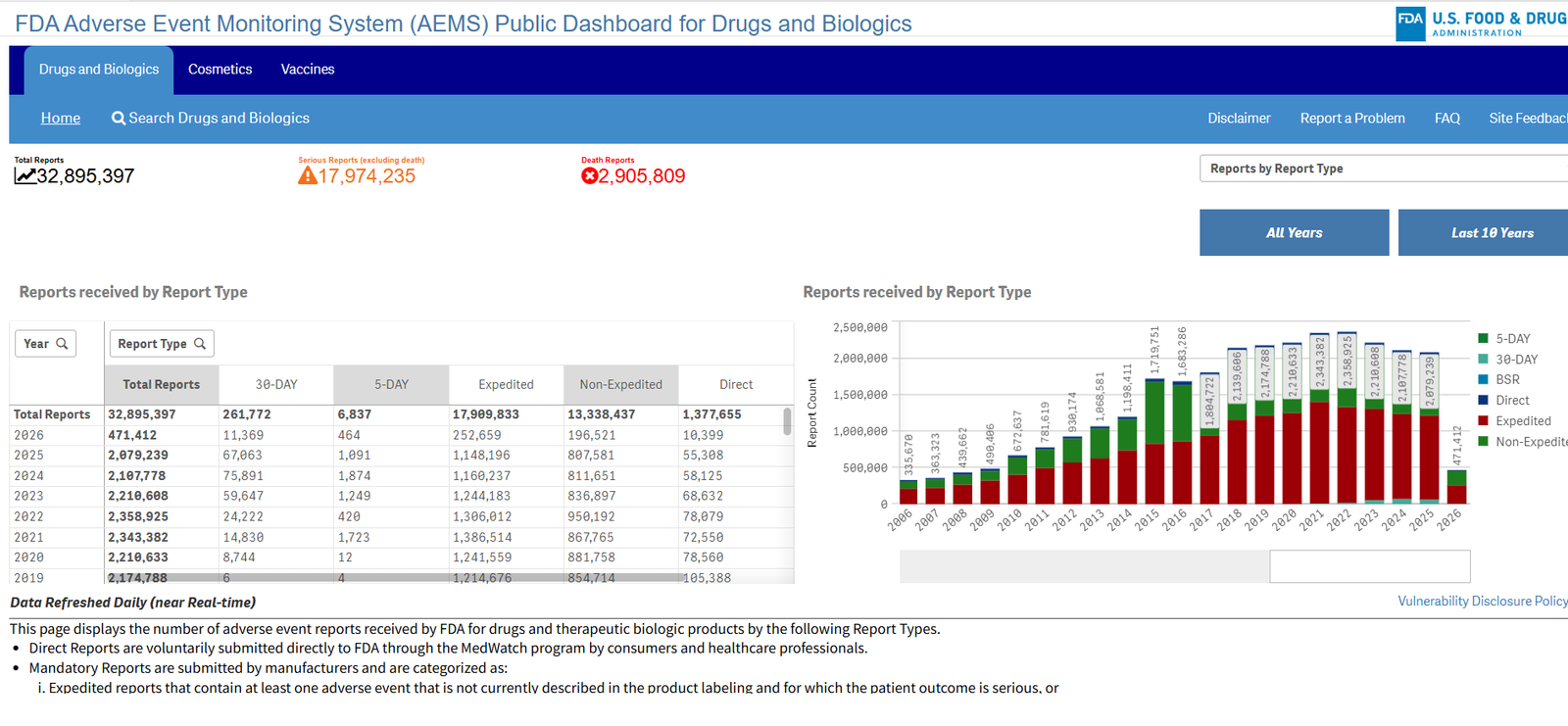
2026年3月11日、米国食品医薬品局(FDA)は正式に、次のようなサービスを開始すると発表した。 有害事象モニタリングシステム(AEMS). .この全く新しい統一プラットフォームとインタラクティブな公開データ・ダッシュボードは、有害事象報告をより効率的に分析・処理するために設計されている。.
システムは年末までにフル稼働する予定である。 2026年5月. .この移行は、業界の状況や一般の人々がデータにアクセスする方法に大きな変化をもたらすだろう。以下は、あなたが知っておくべきコアな情報です:
統一」の時代:すべての規制対象製品をカバー
AEMSの立ち上げは、FDAのデータ統合の取り組みにおける大きな節目となる。AEMSは、FDAが規制するすべての製品カテゴリーにわたって、以下のようなリアルタイムの有害事象報告を提供する:
- 医療製品と医療機器
- ワクチン
- タバコ製品
- 食品と化粧品
- 動物用医薬品
レガシーシステムの引退
この統合を達成するために、FDAは様々なセンターにわたるいくつかの老朽化した分散型報告システムを廃止する。新しいAEMSは、以下のよく知られたプラットフォームを直接置き換えることになる:
- FAERS: 以前は医薬品、生物学的製剤、化粧品、着色料に関する報告に使用されていた。.
- VAERS: 以前はワクチン関連の事件で使用されていた。.
- AERS: 以前は動物用医薬品や動物用食品に使用されていた。.
これらのシステムを単一のプラットフォームに統合することで、FDAは報告プロセスを合理化し、製品横断的な規制監督を強化することを目指している。.
効率化とコスト削減:$1億2,000万ドルの節約と機能拡張
AEMSは有害事象の中核データベースとしての役割を果たすだけでなく、その運用範囲を拡大し、集中管理ハブとなる。AEMSは、消費者からの苦情、規制違反報告、FDAの各センターからの内部告発の処理を一元化する。.
この構想には2つの大きなメリットがある:
- 大幅なコスト削減: FDAは、機能を統合し、レガシーシステムを停止することにより、約 $1億2000万ドル を今後5年間で削減する予定である。.
- 透明性の向上: これまでは、一般の人は四半期ごとにしかデータにアクセスできなかった。AEMSの公開ダッシュボードでは、以下のことが可能になる。 ほぼリアルタイム データ公開。FDAはこれにより、データに対する情報公開法(FOIA)の要求量が大幅に減少することを期待している。.
使用法と重要な “免責事項”
FDA AEMS公開ダッシュボードの展開により、一般市民、医療提供者、業界関係者は有害事象情報の検索にシームレスにアクセスできるようになる。.
重要な注意事項(FDAの公式制限ステートメント) データへのアクセスは容易になったが、FDAはこのデータを解釈する際にいくつかの重要な限界があることを強調している:
- 因果関係はない: システムに有害事象報告があるからといって、その製品がその事象を「引き起こした」ことにはならない。.
- 未確認データ: このシステムに提出された情報は、FDAによって独自に検証されたものではない。.
- 潜在的なデータの欠陥: データベースには、重複提出や不完全なレポートが含まれている可能性があります。.
- 発生率の計算ができない: このデータはモニタリングの参考となるものであり、有害事象の正確な発生率を推測したり、確定したりするものではない。.
AEMSの導入は、デジタルトランスフォーメーションとデータの透明化に向けたFDAの旅における重要なマイルストーンである。製薬会社、研究開発機関、そして一般市民にとって、よりタイムリーなデータは迅速な対応とリスク管理能力の強化を意味する。我々は、5月下旬の完全導入後もシステムのパフォーマンスを監視していく!