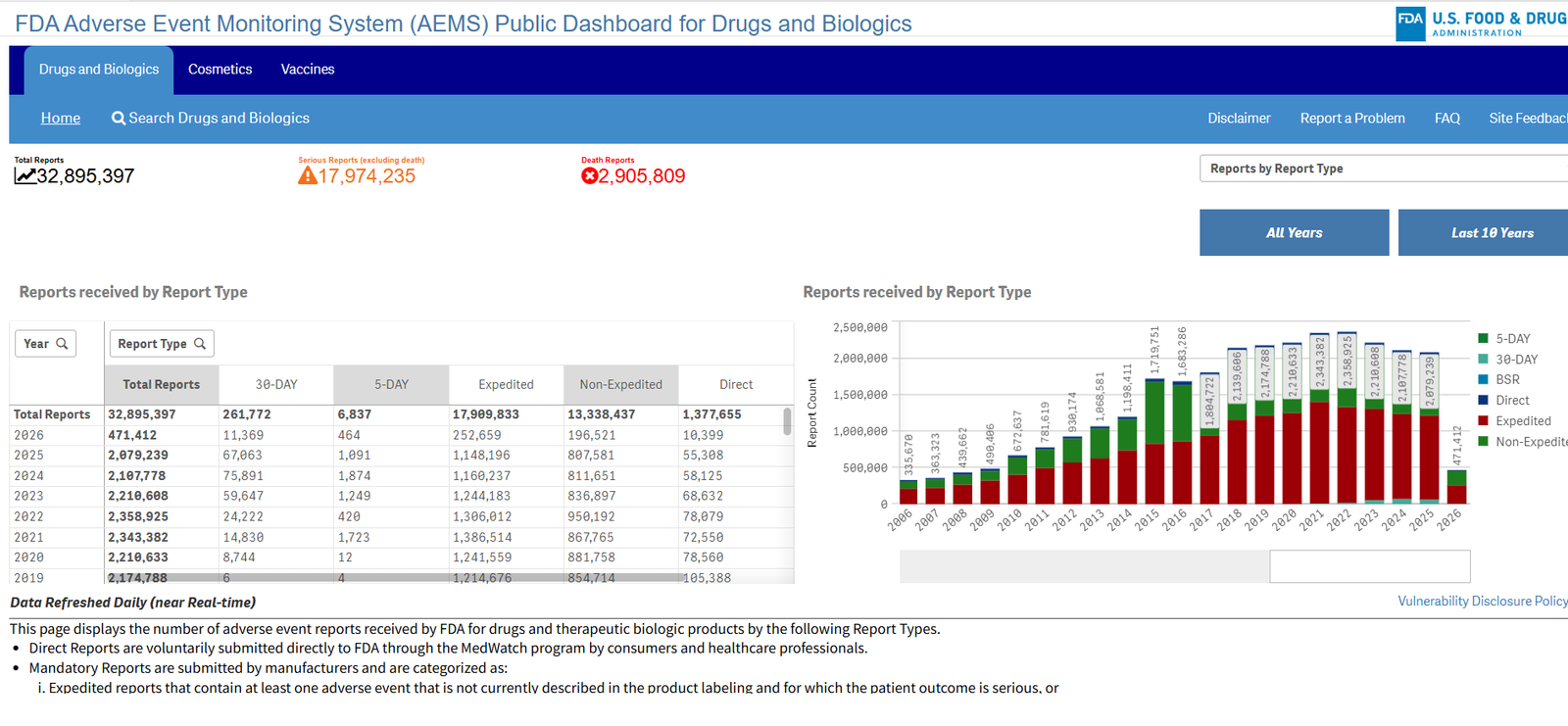
L'11 marzo 2026, la Food and Drug Administration (FDA) degli Stati Uniti ha annunciato ufficialmente il lancio della Sistema di monitoraggio degli eventi avversi (AEMS). Questa nuovissima piattaforma unificata e il dashboard interattivo dei dati pubblici sono stati progettati per analizzare ed elaborare le segnalazioni di eventi avversi con maggiore efficienza.
La piena operatività del sistema è prevista entro la fine di Maggio 2026. Questa transizione porterà cambiamenti significativi nel panorama del settore e nel modo in cui il pubblico accede ai dati. Ecco le informazioni principali da sapere:
Un'era “unificata”: Copertura di tutti i prodotti regolamentati
Il lancio di AEMS segna un'importante pietra miliare negli sforzi di integrazione dei dati della FDA. Fornirà la segnalazione di eventi avversi in tempo reale per tutte le categorie di prodotti regolamentati dalla FDA, tra cui:
- Prodotti e dispositivi medici
- Vaccini
- Prodotti del tabacco
- Alimenti e cosmetici
- Farmaci veterinari
Ritiro dei sistemi legacy
Per realizzare questa integrazione, la FDA smantellerà diversi sistemi di reporting decentralizzati e obsoleti in vari centri. Il nuovo AEMS sostituirà direttamente le seguenti piattaforme ben note:
- FAER: Precedentemente utilizzato per la segnalazione di farmaci, prodotti biologici, cosmetici e additivi colorati.
- VAERS: Precedentemente utilizzato per gli incidenti legati ai vaccini.
- AERS: In passato è stato utilizzato per farmaci e alimenti per animali.
Consolidando questi sistemi in un'unica piattaforma, l'FDA mira a snellire il processo di segnalazione e a migliorare il controllo normativo su più prodotti.
Efficienza e risparmio: $120 milioni di euro risparmiati e funzionalità ampliate
Oltre a fungere da database principale per gli eventi avversi, l'AEMS amplierà la sua portata operativa per diventare un hub di gestione centralizzato. Unificherà l'elaborazione dei reclami dei consumatori, delle segnalazioni di violazioni normative e delle denunce provenienti da diversi centri della FDA.
Questa iniziativa offre due vantaggi principali:
- Massicci risparmi sui costi: L'FDA stima che consolidando le funzioni e chiudendo i sistemi esistenti, circa $120 milioni nei prossimi cinque anni si risparmierà sui costi operativi.
- Maggiore trasparenza: In precedenza, il pubblico poteva accedere ai dati solo su base trimestrale. Ora, il cruscotto pubblico di AEMS consentirà di quasi in tempo reale pubblicazione dei dati. L'FDA prevede che questo ridurrà in modo significativo il volume delle richieste di dati da parte del Freedom of Information Act (FOIA).
Utilizzo e importanti “disclaimer”
Con l'introduzione del dashboard pubblico dell'FDA AEMS, il pubblico, gli operatori sanitari e i professionisti del settore avranno un accesso continuo alla ricerca di informazioni sugli eventi avversi.
Promemoria critico (Dichiarazione ufficiale della FDA sulle limitazioni) Sebbene l'accesso ai dati sia diventato più semplice, l'FDA sottolinea alcune limitazioni fondamentali nell'interpretazione di questi dati:
- Nessuna causalità implicita: La presenza di una segnalazione di evento avverso nel sistema non significa che il prodotto abbia “causato” l'evento.
- Dati non verificati: Le informazioni inviate al sistema non sono state verificate in modo indipendente dalla FDA.
- Potenziali difetti dei dati: Il database potrebbe contenere duplicati o segnalazioni incomplete.
- Impossibilità di calcolare l'incidenza: Questi dati servono solo come riferimento per il monitoraggio e non possono essere utilizzati per dedurre o stabilire l'esatto tasso di incidenza degli eventi avversi.
L'introduzione dell'AEMS è una pietra miliare significativa nel percorso della FDA verso la trasformazione digitale e la trasparenza dei dati. Per le aziende farmaceutiche, gli istituti di ricerca e sviluppo e il pubblico, dati più tempestivi significano tempi di risposta più rapidi e maggiori capacità di gestione del rischio. Continueremo a monitorare le prestazioni del sistema dopo la sua completa implementazione a fine maggio!