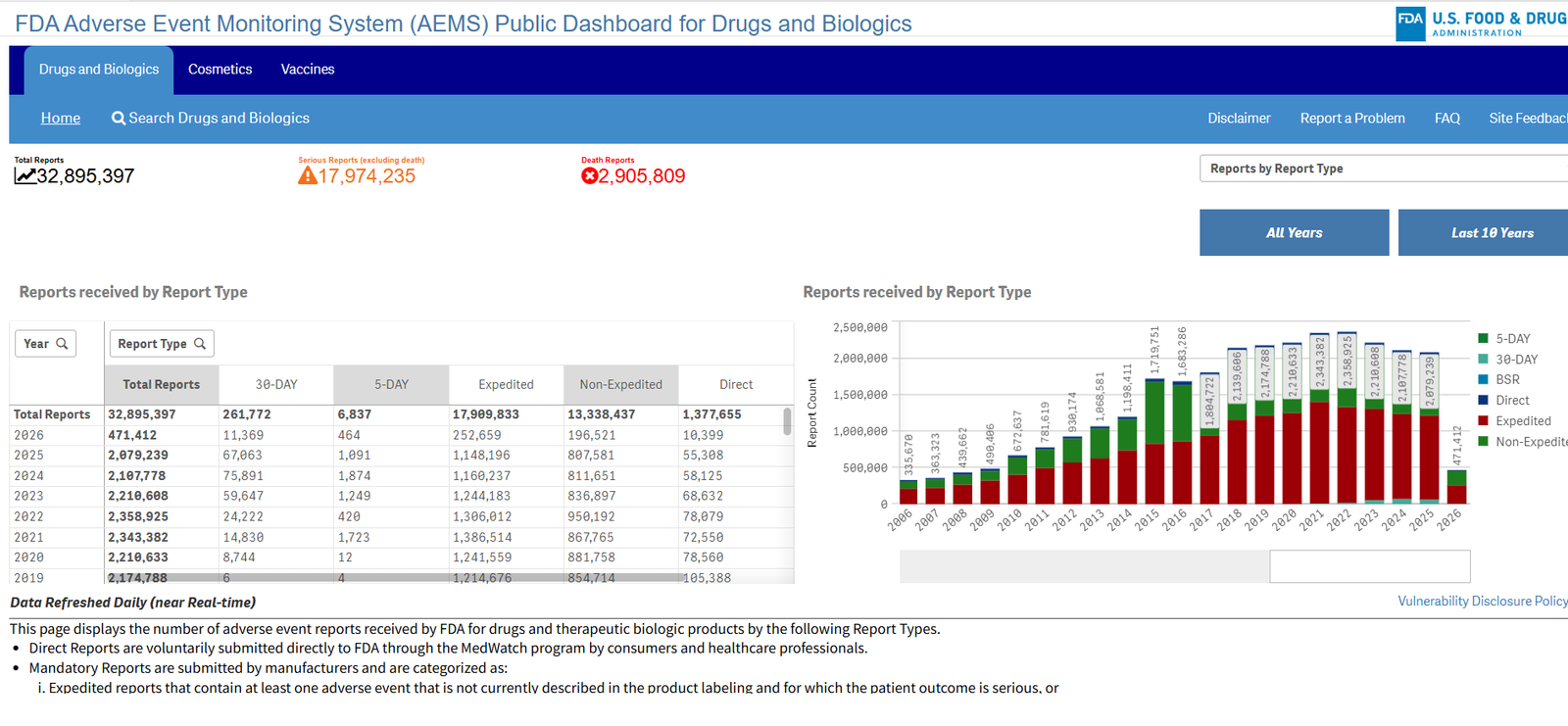
Em 11 de março de 2026, a Food and Drug Administration (FDA) dos EUA anunciou oficialmente o lançamento da Sistema de Monitorização de Eventos Adversos (AEMS). Esta novíssima plataforma unificada e o painel de dados público interativo foram concebidos para analisar e processar as notificações de eventos adversos com maior eficiência.
Prevê-se que o sistema esteja totalmente operacional até ao final de maio de 2026. Esta transição trará alterações significativas ao panorama do sector e à forma como o público acede aos dados. Eis as principais informações que precisa de saber:
Uma era “unificada”: Abrangendo todos os produtos regulamentados
O lançamento do AEMS constitui um marco importante nos esforços de integração de dados da FDA. O AEMS fornecerá relatórios de eventos adversos em tempo real em todas as categorias de produtos regulamentados pela FDA, incluindo:
- Produtos e dispositivos médicos
- Vacinas
- Produtos do tabaco
- Alimentos e cosméticos
- Medicamentos veterinários
Retirada de sistemas legados
Para conseguir esta integração, a FDA irá desativar vários sistemas de notificação antigos e descentralizados em vários centros. O novo AEMS substituirá diretamente as seguintes plataformas bem conhecidas:
- FAERS: Anteriormente utilizado para a comunicação de dados sobre medicamentos, produtos biológicos, cosméticos e aditivos corantes.
- VAERS: Anteriormente utilizado para incidentes relacionados com vacinas.
- AERS: Anteriormente utilizado para medicamentos e alimentos para animais.
Ao consolidar estes sistemas numa única plataforma, a FDA pretende simplificar o processo de comunicação e melhorar a supervisão regulamentar entre produtos.
Eficiência e redução de custos: $120 milhões poupados e funcionalidade alargada
Para além de servir como base de dados central para eventos adversos, a AEMS irá expandir o seu âmbito operacional para se tornar um centro de gestão centralizado. Unificará o processamento de queixas dos consumidores, relatórios de infracções regulamentares e denúncias de diferentes centros da FDA.
Esta iniciativa apresenta duas grandes vantagens:
- Poupança maciça de custos: A FDA estima que, através da consolidação de funções e do encerramento de sistemas antigos, cerca de $120 milhões em custos de funcionamento serão poupados nos próximos cinco anos.
- Maior transparência: Anteriormente, o público só podia aceder aos dados numa base trimestral. Agora, o painel de controlo público da AEMS permitirá quase em tempo real publicação de dados. A FDA espera que esta medida reduza significativamente o volume de pedidos de dados no âmbito da Lei da Liberdade de Informação (FOIA).
Utilização e “Avisos legais” importantes”
Com o lançamento do painel de controlo público da FDA AEMS, o público em geral, os prestadores de cuidados de saúde e os profissionais do sector terão um acesso fácil à pesquisa de informações sobre eventos adversos.
Lembrete crítico (Declaração oficial de limitações da FDA) Embora o acesso aos dados se tenha tornado mais fácil, a FDA salienta várias limitações importantes na interpretação destes dados:
- Não há causalidade implícita: A presença de um relatório de evento adverso no sistema não significa que o produto “causou” o evento.
- Dados não verificados: As informações submetidas ao sistema não foram verificadas de forma independente pela FDA.
- Potenciais falhas de dados: A base de dados pode conter duplicados ou relatórios incompletos.
- Incapacidade de calcular a incidência: Estes dados servem apenas como referência para monitorização e não podem ser utilizados para inferir ou estabelecer a taxa de incidência exacta de acontecimentos adversos.
A introdução do AEMS é um marco significativo no percurso da FDA em direção à transformação digital e à transparência dos dados. Para as empresas farmacêuticas, as instituições de I&D e o público, dados mais atempados significam tempos de resposta mais rápidos e capacidades de gestão de risco mais fortes. Continuaremos a monitorizar o desempenho do sistema após a sua implementação total no final de maio!