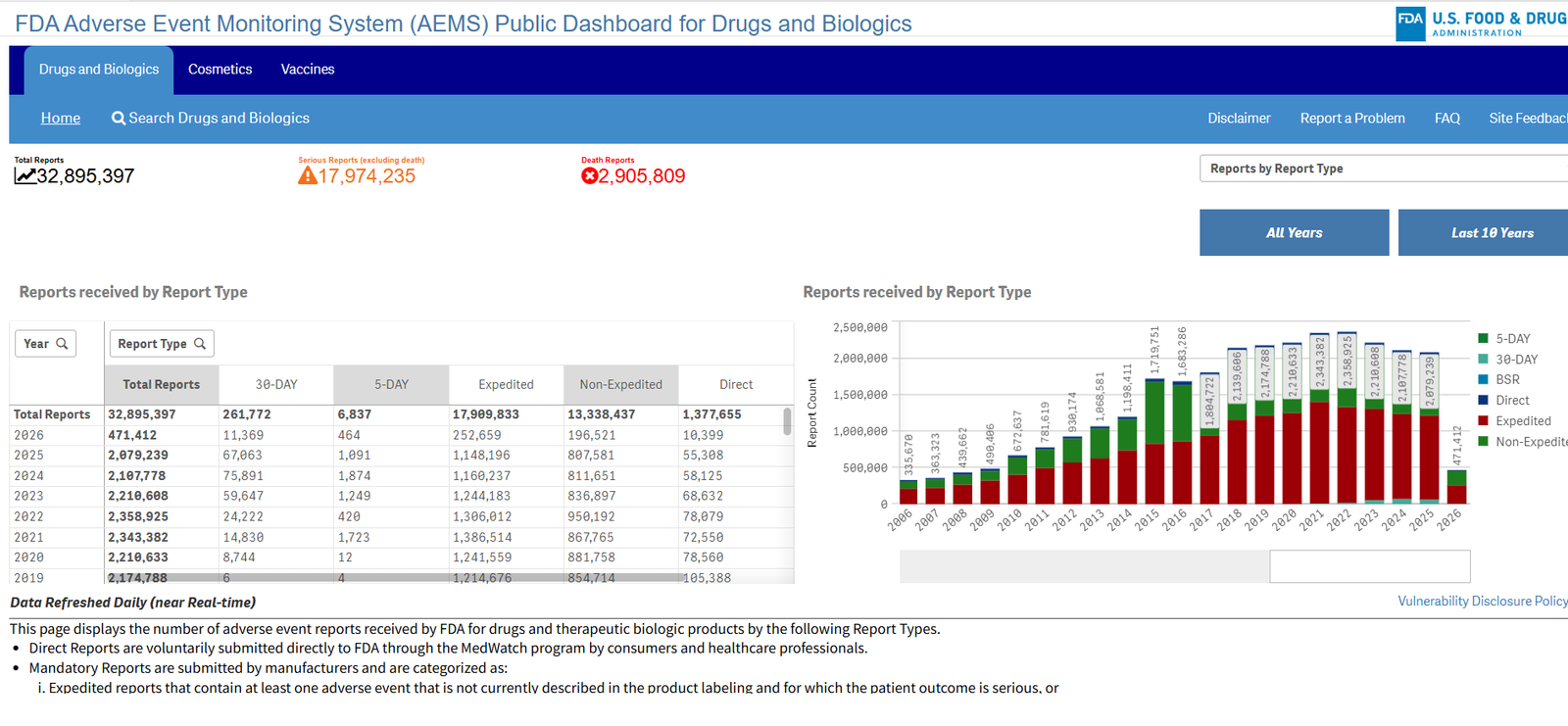
2026년 3월 11일, 미국 식품의약국(FDA)은 공식적으로 다음과 같이 발표했습니다. 부작용 모니터링 시스템(AEMS). 이 새로운 통합 플랫폼과 대화형 공개 데이터 대시보드는 부작용 보고서를 보다 효율적으로 분석하고 처리할 수 있도록 설계되었습니다.
이 시스템은 연말까지 완전히 가동될 예정입니다. 2026년 5월. 이러한 전환은 업계 환경과 대중이 데이터에 액세스하는 방식에 큰 변화를 가져올 것입니다. 다음은 여러분이 알아야 할 핵심 정보입니다:
“통합” 시대: 모든 규제 대상 제품 포함
AEMS의 출시는 FDA의 데이터 통합 노력에 있어 중요한 이정표가 될 것입니다. 이 솔루션은 다음을 포함한 모든 FDA 규제 대상 제품 범주에 걸쳐 실시간 부작용 보고 기능을 제공합니다:
- 의료 제품 및 장치
- 백신
- 담배 제품
- 식품 및 화장품
- 동물 의약품
레거시 시스템 폐기
이러한 통합을 달성하기 위해 FDA는 여러 센터에 분산되어 있는 노후화된 여러 보고 시스템을 폐기할 예정입니다. 새로운 AEMS는 다음과 같이 잘 알려진 플랫폼을 직접 대체할 것입니다:
- FAERS: 이전에는 의약품, 생물학적 제품, 화장품 및 색소 첨가제에 대한 보고에 사용되었습니다.
- VAERS: 이전에는 백신 관련 사건에 사용되었습니다.
- AERS: 이전에는 동물용 의약품과 동물 사료에 사용되었습니다.
이러한 시스템을 단일 플랫폼으로 통합함으로써 FDA는 보고 프로세스를 간소화하고 제품 간 규제 감독을 강화하는 것을 목표로 합니다.
효율성 및 비용 절감: $120백만 절감 및 기능 확장
AEMS는 부작용에 대한 핵심 데이터베이스 역할을 넘어 중앙 집중식 관리 허브로 운영 범위를 확장할 예정입니다. 여러 FDA 센터에서 접수되는 소비자 불만, 규정 위반 신고, 내부 고발자 제보를 통합하여 처리할 예정입니다.
이 이니셔티브는 두 가지 주요 이점을 제공합니다:
- 막대한 비용 절감: FDA는 기능을 통합하고 레거시 시스템을 종료함으로써 대략 다음과 같이 추정합니다. $1억2천만 의 운영 비용을 향후 5년간 절감할 수 있습니다.
- 투명성 향상: 이전에는 일반인이 분기 단위로만 데이터에 액세스할 수 있었습니다. 이제 AEMS 공개 대시보드에서 다음을 수행할 수 있습니다. 실시간에 가까운 데이터 게시. FDA는 이를 통해 데이터에 대한 정보 자유법(FOIA) 요청의 양이 크게 줄어들 것으로 예상하고 있습니다.
사용 및 중요한 “면책 조항”
FDA AEMS 공개 대시보드가 출시되면 일반 대중, 의료 서비스 제공자 및 업계 전문가가 부작용 정보를 원활하게 검색할 수 있게 됩니다.
중요 알림(FDA 공식 제한 사항) 데이터 액세스는 더 쉬워졌지만, FDA는 이 데이터를 해석할 때 몇 가지 주요 제한 사항을 강조합니다:
- 인과관계가 암시되지 않습니다: 시스템에 부작용 보고서가 있다고 해서 해당 제품이 부작용을 “유발'했다는 의미는 아닙니다.
- 확인되지 않은 데이터: 시스템에 제출된 정보는 FDA에서 독립적으로 검증되지 않았습니다.
- 잠재적인 데이터 결함: 데이터베이스에 중복 제출 또는 불완전한 보고서가 포함될 수 있습니다.
- 발생률을 계산할 수 없습니다: 이 데이터는 모니터링을 위한 참고 자료로만 사용되며 부작용의 정확한 발생률을 추론하거나 확정하는 데 사용할 수 없습니다.
AEMS의 도입은 디지털 혁신과 데이터 투명성을 향한 FDA의 여정에서 중요한 이정표입니다. 제약회사, R&D 기관, 그리고 일반 대중에게 시기적절한 데이터는 더 빠른 대응 시간과 더 강력한 위험 관리 역량을 의미합니다. 5월 말 전면 시행 이후에도 시스템의 성과를 지속적으로 모니터링할 예정입니다!