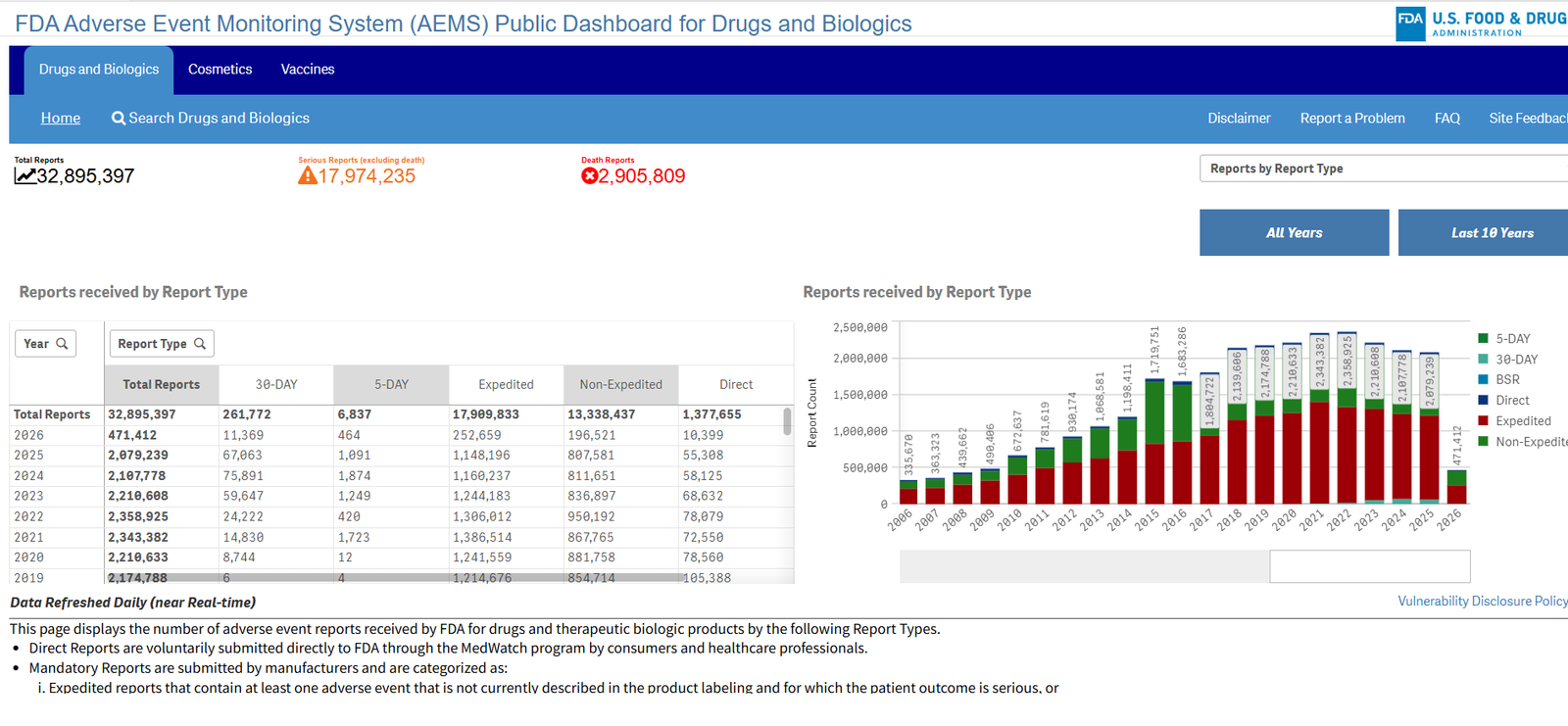
El 11 de marzo de 2026, la Administración de Alimentos y Medicamentos de EE.UU. (FDA) anunció oficialmente el lanzamiento del Sistema de vigilancia de acontecimientos adversos (AEMS). Esta flamante plataforma unificada y panel público interactivo de datos está diseñada para analizar y procesar los informes de efectos adversos con mayor eficacia.
Está previsto que el sistema esté plenamente operativo a finales de Mayo de 2026. Esta transición supondrá cambios significativos en el panorama del sector y en la forma en que el público accede a los datos. He aquí la información básica que debe conocer:
Una era “unificada”: Todos los productos regulados
El lanzamiento de AEMS marca un hito importante en los esfuerzos de integración de datos de la FDA. Proporcionará información en tiempo real sobre acontecimientos adversos en todas las categorías de productos regulados por la FDA, incluidos:
- Productos y dispositivos médicos
- Vacunas
- Productos del tabaco
- Alimentación y cosmética
- Medicamentos veterinarios
Retirada de los sistemas heredados
Para lograr esta integración, la FDA desmantelará varios sistemas de notificación anticuados y descentralizados en varios centros. El nuevo AEMS sustituirá directamente a las siguientes plataformas bien conocidas:
- FAERS: Antes se utilizaba para informar sobre medicamentos, productos biológicos, cosméticos y aditivos colorantes.
- VAERS: Anteriormente se utilizaba para incidentes relacionados con vacunas.
- AERS: Antiguamente se utilizaba para medicamentos y alimentos para animales.
Al consolidar estos sistemas en una única plataforma, la FDA pretende agilizar el proceso de notificación y mejorar la supervisión reglamentaria de los distintos productos.
Eficiencia y ahorro de costes: $120 millones ahorrados y funcionalidad ampliada
Además de servir como base de datos central de acontecimientos adversos, el AEMS ampliará su ámbito operativo para convertirse en un centro de gestión centralizada. Unificará la tramitación de las reclamaciones de los consumidores, los informes sobre infracciones normativas y las denuncias de los distintos centros de la FDA.
Esta iniciativa ofrece dos grandes ventajas:
- Ahorro masivo de costes: La FDA calcula que, mediante la consolidación de funciones y el cierre de los sistemas heredados, aproximadamente $120 millones en gastos de funcionamiento en los próximos cinco años.
- Mayor transparencia: Antes, el público sólo podía acceder a los datos trimestralmente. Ahora, el panel público de AEMS permitirá casi en tiempo real publicación de datos. La FDA espera que esto reduzca significativamente el volumen de solicitudes de datos en virtud de la Ley de Libertad de Información (FOIA).
Uso y “descargos de responsabilidad” importantes”
Con la puesta en marcha del panel público AEMS de la FDA, el público en general, los profesionales sanitarios y los profesionales de la industria tendrán un acceso sin fisuras a la búsqueda de información sobre acontecimientos adversos.
Recordatorio crítico (Declaración oficial de limitaciones de la FDA) Aunque el acceso a los datos es ahora más fácil, la FDA hace hincapié en varias limitaciones clave a la hora de interpretar estos datos:
- No hay causalidad implícita: La presencia de un informe de efecto adverso en el sistema no significa que el producto “causara” el efecto.
- Datos no verificados: La información enviada al sistema no ha sido verificada de forma independiente por la FDA.
- Posibles fallos en los datos: La base de datos puede contener envíos duplicados o informes incompletos.
- Incapacidad para calcular la incidencia: Estos datos sirven únicamente como referencia para el seguimiento y no pueden utilizarse para deducir o establecer la tasa exacta de incidencia de acontecimientos adversos.
La introducción de AEMS es un hito importante en el camino de la FDA hacia la transformación digital y la transparencia de los datos. Para las empresas farmacéuticas, las instituciones de I+D y el público en general, unos datos más oportunos significan tiempos de respuesta más rápidos y una mayor capacidad de gestión de riesgos. Seguiremos supervisando el rendimiento del sistema tras su plena implantación a finales de mayo.